|
VÝZKUM 2003 |
26.12.2003
·
Christmas
gift: Youngest artificial patient survives
23.12.2003
·
Negamycin
obnovuje tvorbu dystrofinu v kosterním svalstvu a srdci u mdx myší
Arakawa M, Shiozuka M,
Nakayama Y, Hara T, Hamada M, Kondo S, Ikeda D, Takahashi Y, Sawa R, Nonomura
Y, Sheykholeslami K, Kondo K, Kaga K, Kitamura T, Suzuki-Miyagoe Y, Takeda S,
Matsuda R.; Department of Life Sciences, The University of Tokyo, 3-8-1 Komaba,
Tokyo 153-8902.
Známá schopnost aminoglykosidových
antibiotik umožnit přečtení genu i v případě některých typů nesmyslných (nonsense) mutací přitahuje
pozornost badatelů jako potenciální lék na genetické poruchy. Avšak toxicita
aminoglykosidových antibiotik může při dlouhodobém užíváni vést k vážným
vedlejším problémům. Bylo zjištěno, že negamycin, dipeptidové antibiotikum,
také obnovuje tvorbu dystrofinu v kosternim svalstvu a srdci u mdx myší a v
laboratorně pěstovaných svalových vláknech mdx myší. Tvorba dystrofinu byla
potvrzena imunohistochemicky i metodou immunoblotting*. Také jsme
provedli porovnání toxicity negamycinu a gentamycinu a zjistili, že negamycin
je méně toxický. Vědci
dospěli k přesvědčení, že negamycin je slibný kandidát pro léčbu DMD a jiných
genetických poruch způsobených nonsense mutacemi.
21.12.2003
·
BRAZILIAN
RESEARCH CENTER - IMPORTANT INFORMATIONS
V brazilském Ribeirao Preto, asi 250 mil od São Paulo, vzniklo Genetic Therapy Center (CTG). Založilo jej brazilské sdružení rodičů Association of Friends of DMD (AADM) s cílem studovat léky na mdx myších ( kmen myši s delecí na dystrofinovém genu ) a GRMD psech ( zlatý retriever, kmen s poškozením dystrofinového genu ). Ředitelkou AADM i CTG je paní Edna Maria Pupin, jejíž 25 letý syn trpí DMD. Šéfem výzkumu je doktor David Feder, otec 13 letého chlapce s DMD. Spolupráci s CTG slíbili odborníci z Británie, Francie, Německa a USA, s CTG spolupracuje University of Ribeirao Preto, po rozšíření výkumu se předpokládá spolupráce i s University of Sao Paulo.
Centrum bylo vybudováno a vybaveno
z peněz fondů rodičů a Fapesp (State of São Paulo Research Foundation ). Hlavním a jediným cílem tohoto výzkumného
centra je studovat svalovou dystrofii. Pro udržení CTG v chodu v nejbližších
třech letech je potřeba 10 milionů USD. Proto CTG oslovuje velké firmy, nadace
i jedince s žádostí o finanční podporu. Pokud má někdo zájem podpořit CTG může
kontaktovat :
·
Dr.
Arnold H. Pelofsky, PhD, email : aerenter@comcast.net
· Edna Maria Pupin, email : aadm@aadm.com.br; adresa : Av. Bandeirantes, 2419; Vila Virginia, Ribeirao Preto, SP, Brazil; 14030-670.
Všechny léky, které mají být zkoumány, jsou již na trhu a schválené FDA ( U.S. Food and Drug Administration ). Každý lék, který bude testován, má určitou vlastnost, která, jak odborníci z CTG doufají, může pomoct zmírnit symptomy této hrozné choroby. Léky budou nejdříve testovány na mdx myších a GRDM psech. Farmaceutické firmy, vyrábějící příslušné léky, již ukončily studie bezpečnosti na zvířatech ale odmítly dát jejich výsledky CTG. Jestliže testy na zvířatech ukáží pozitivní výsledky bez příliš závažných vedlejších efektů, provedou se klinické studie podle příslušných brazilských zákonů a budou iniciovány i pokusy po celém světě s cílem ověřit správnost výsledků.
Od začátku devadesátých let jsou ke zpomalení postupu nemoci používány steroidy, ty ale mají mnoho nepříznivých vedlejších efektů. Odborníci z CTG se domnívají, že jestliže steroidy mají pozitivní efekt, musí existovat i jiné účinné léky, které ale nebudou mít negativní vedlejší účinky jako steroidy. Výzkum se bude týkat těchto látek :
·
Mitochondrial stabilizing/enhancing
compounds*
·
Plasma membrane stabilizers
·
Calcium reduction agents
·
Fibrosis reducing agents
·
Agents that oxygenate affected
skeletal muscle tissues
Všechny nové informace o výsledcích pokusů ( dobré i špatné ), jména výzkumníků, poradců, sponzorů, názvy
léků, jak je projekt financován, atd. to vše bude publikováno na nově vznikajících www stránkach
na adrese : http://www.fightforafuture.org.
Pár fotografií z výstavbyCTG centra :
· http://www.distrofiamuscular.net/researchcenter.htm
· http://www.distrofiamuscular.net/researchcenter1.htm
· http://www.distrofiamuscular.net/researchcenter2.htm
20.12.2003
· Scientists
looking at potential to 'repair' heart muscles
· Stimulation
of calcineurin signaling attenuates the dystrophic pathology in mdx mice
· Antisense-Induced
Multiexon Skipping for Duchenne Muscular Dystrophy Makes More Sense
· Stem cell therapy for muscular dystrophy
18.12.2003
· Therapeutics
for Duchenne muscular dystrophy: current approaches and future directions
( Celý tento článek právě
vyšel v Journal of
Molecular Medicine,
cena článku je 35.-USD. Pokud již někdo má tento článek budeme rádi když nám
pošlete kopii. Děkujeme. )
· Muscle-derived
stem cells: potential for muscle regeneration.
17.12.2003
Kompletní analýza dystrofinového genu
provedená pomocí techniky DOVAM
City of Hope National Medical Center in
Duarte, Calif.
Analýza dystrofinového genu - Institut HOPE
Identifikace kauzativních mutací v dystrofinovém genu pro rodiny
sledované pro výskyt DMD nebo BMD může poskytnout přesnou diagnózu bez nutnosti
podstoupit svalovou biopsii. Rozpoznání mutace a její velmi přesné určení poskytne
informace pro tzv. prenatální diagnózu u ženy přenašečky.
Pro pacienty, u nichž nebyla objevena velká delece (chybějící exon) je
určena úplná analýza mutací v dystrofinovém genu. Po odhalení těchto mutací je
možné sestavit prenatální diagnózu pro rodinu, kde se vyskytlo dítě s DMD nebo
BMD.
Údaje pro testování
Jednotlivce s možnou diagnózou DMD nebo BMD, příbuzní ženského pohlaví a
pacienti s DMD/BMD jsou vhodnými kandidáty pro testy.
Metody testu:
1.Deleční analýza - PCR rozlišení
bude provedeno pro 26 exonů (z celkového počtu 79), u kterých je nejčastější
přítomnost delecí.
2. Úplná analýza mutací -
pokud nebude odhalena velká delece, budou analyzovány všechny kódovací oblasti
(křižovatky dystrofinového genu) pomocí
sekvenční DNA analýzy.
Samotný test
1.
Deleční analýza - pro 26 testovaných
exonů v dystrofinovém genu bude úspěšnost odhalení u pacientů s DMD nebo BMD
větší než 99% s přesností větší než 97 %. Velká vymazání exonů mimo
prověřovaných 26 nebude touto metodou odhaleno, ale bude je mažné najít pomocí
úplné analýzy mutací. Přesnost a specifikace pro prenatální diagnostiku bude
větší než 99%.
2. Úplná analýza mutací - pokud bude mutace přítomna v oblasti snímané pomocí testu, bude
stanovena s přesností větší než 97%. Bodové mutace by měly být rozpoznány u 75%
případů DMD, kde nebyla dosud delece odhalena. Mnohonásobné faktory včetně
genetické různorodosti a existence mutací mimo oblast pravděpodobného výskytu
mohou být důvodem pro nenalezení mutací u ostatních pacientů. Nicméně společně
analýza a úplná analýza mutací objeví příčiny DMD nebo BMD u 90% pacientů.
Shrnutí
Deleční analýza odhalí delece u 26 exonů, úplná mutační analýza neobjeví
velká zdvojování (asi 5% případů) nebo mutace mimo analyzované oblasti.
Úplná analýza mutací může objevit velká vymazání u mužských pacientů,
ale ne u žen.
Doručení krevního vzorku do 72 hodin (cena testu 900 - 1600 dolarů , výsledky asi za 18
týdnů), více informací na:
15.12.2003
Nové testy dokáží odhalit mnohem víc poruch v
dystrofinovém genu
Dystrofinový gen, který nese informace pro tvorbu
dystrofinu a je u DMD a BMD poškozen,
je extrémně dlouhý komplex pro genetické testování.
V současné době výzkumníci podporovaní MDA vyvinuli
nové testy, které umožní objevit mnohem vyšší procento mutací včetně méně
významných změn, které přesto způsobují tuto nemoc. Dostupné testy můžou
odhalit jenom ty typy mutací, které představují nepřítomnost celkem rozsáhlých
kusů genu - tzv. „delecí“. Tyto deleční nalýzy lze aplikovat jen u 60% pacientů
s DMD a nějakého procenta s BMD.
TEST BAYLOR
Carolyn Sue Richards, molekulární bioložka a vědci z Vysoké škola Baylor
v Houstonu pracují na typu analýzy dystrofinového genu založeném na DHPLC
technice. Klinický pokus chce ověřit test na skupině nejméně 100 chlapců s
klinickými příznaky DMD nebo BMD, u kterých nebyla odhalena žádná delece a diagnóza byla potvrzena na základě svalové
biopsie. Informace, jak se lze dostat do této studie je kontakt dsl@bcm.tmc.edu (… není nutná cesta do Houstonu)
Test
na Univerzitě v Utahu
Kevin Flanigan, podporovaný MDA z Univerzity v Utahu, Salt Lake City, byl
ve skupině, která nedávno vyvinula další přístup, který dokáže zkvalitnit
genetické testy. Ředitel kliniky MDA v Ohio nabízí pacientům vyzkoušet tento
nový test. Očekává se, že test bude dostupný za cenu nižší než 1000 dolarů
14.12.2003
·
Aktivní granty MDAUSA (
Asociace svalových dystrofiků USA ) pro rok 2003
(
Článek
popisuje metodu, kterou vyvíjí a začíná klinicky zkoušet Dr. Matsuo z Kobe
University Graduate School of Medicine. Článek navazuje na informaci Doctor
claims DNA treatment for Duchenne muscular dystrophy z 6.12.2003 )
6.12.2003
·
NaPro Awarded
Phase I SBIR Grant for Research on Muscular Dystrophy
· Doctor claims DNA treatment for Duchenne muscular dystrophy
Transplantace
normálních a geneticky pozměněných myoblastů
Tremblay Jacques
 Cílem laboratoře Dr. Tremblaye je vyvinout
lečbu Duchenneovy svalové dystrofie (DMD). Tato dědičná choroba
je charakteristická postupným slábnutím kosterního svalstva. Slabost se stává
zřetelnou ve věku 5 let, kdy pacienti začínají mít problémy s chůzí. Od 10
let jsou pacienti odkázáni na vozík. Smrt nastává mezi 17 a 23 rokem
z důvodu zeslábnutí dýchacího svalstva. Gen odpovědný za tuto chorobu byl identifikován
v roce 1987. Tento gen kóduje velkou bílkovinu zvanou dystrofin, která je
umístěna v pod membránou svalového vlákna. Absence tohoto proteinu činí vlákna
zranitelnými při fyzické zátěži. V případě poškození se na místě svalových vláken namnoží malé buňky zvané
myoblasty a „opraví“ je. Myoblasty se nachází okolo každého svalového vlákna.
Naneštěstí opravená vlákna stále nedokáží vytvářet dystrofin a jsou brzy opět
poškozena. Tento cyklus
degenerace a regenerace vede ke stárnutí myoblastů což vede k snížení
schopnosti opravovat sval a tudíž k slábnutí svalstva. Od objevení
dystrofinu vědci hledají způsob jak obnovit tento protein v v pacientových
svalových vláknech. Od roku 1987 laboratoř Dr. Tremblaye transplantuje normální
myoblasty od dárců do svalů pacientů s DMD. Tato léčba byla zkoumána v letech
1990-1991 ale vedla jen k velmi malému zvýšení dystrofin-positivních vláken a
jen k přechodnému vzrůstu svalové síly u několika pacientů.
Cílem laboratoře Dr. Tremblaye je vyvinout
lečbu Duchenneovy svalové dystrofie (DMD). Tato dědičná choroba
je charakteristická postupným slábnutím kosterního svalstva. Slabost se stává
zřetelnou ve věku 5 let, kdy pacienti začínají mít problémy s chůzí. Od 10
let jsou pacienti odkázáni na vozík. Smrt nastává mezi 17 a 23 rokem
z důvodu zeslábnutí dýchacího svalstva. Gen odpovědný za tuto chorobu byl identifikován
v roce 1987. Tento gen kóduje velkou bílkovinu zvanou dystrofin, která je
umístěna v pod membránou svalového vlákna. Absence tohoto proteinu činí vlákna
zranitelnými při fyzické zátěži. V případě poškození se na místě svalových vláken namnoží malé buňky zvané
myoblasty a „opraví“ je. Myoblasty se nachází okolo každého svalového vlákna.
Naneštěstí opravená vlákna stále nedokáží vytvářet dystrofin a jsou brzy opět
poškozena. Tento cyklus
degenerace a regenerace vede ke stárnutí myoblastů což vede k snížení
schopnosti opravovat sval a tudíž k slábnutí svalstva. Od objevení
dystrofinu vědci hledají způsob jak obnovit tento protein v v pacientových
svalových vláknech. Od roku 1987 laboratoř Dr. Tremblaye transplantuje normální
myoblasty od dárců do svalů pacientů s DMD. Tato léčba byla zkoumána v letech
1990-1991 ale vedla jen k velmi malému zvýšení dystrofin-positivních vláken a
jen k přechodnému vzrůstu svalové síly u několika pacientů.
Od té
doby laboratoř Dr. Tremblaye identifikovala příčiny, které vedly k malé
účinnosti a nyní hledá řešení. První problém je rychlá zánětlivá reakce následující po vnitrosvalové injekci
myoblastů. Tento problém byl redukován na zvířecích modelech použitím protilátky
LFA-1. Druhým problémem je omezená schopnost šíření
injikovaných buňek do mimobuněčné matrice. Dr. Tremblay zkouší vyřešit tento
problém vložením genu pro bílkovinu metalloproteinase ( enzym, který “stravuje”
tyto matrice ) do myoblastu před tím než je transplantován. Třetím problémem je
imunitní reakce na dárcovské buňky. Tento problém je řešen použitím
imunosuprese pacientů pomocí imunosupresoru FK506.
Výzkum vedený týmem Dr. Tremblaye
dosáhl výborných výsledků na zvířatech. U dystrofických myší transplantace
myoblastů vedla k obnově tvorby fystrofinu v 95% svalových vláken. U opic byl pozorován
výskyt „reporter genu“ transplantovaného v myoblastech u víc než 10.000
svalových vláken na cm3.
Transplantace normálních nebo geneticky pozměněných myoblastů může být použita pro léčbu nejen myopatií ale řady jiných vrozených či získaných chorob.
Tyto výzkumy jsou podporovány
organizacemi Muscular Dystrophy Association of Canada a Association française
contre les myopathies.
Poslední informace od Dr.Tremblaye z 1.12.2003 : “Právě
probíhá první fáze klinických
pokusů na DMD pacientech. Dosáhli jsme obnovení tvorby dystrofinu ve svalových
vláknech u prvních tří chlapců účastnících se pokusu. Tyto pozitivní výsledky
budou brzy publikovány v Molecular Therapy. Myoblasty byly vpíchnuty jen do 1
cm3 svalu, takže dystrofin pozitivní vlákna se nachází jen v tomto místě.
Vzhledem k tomu, že myoblasty byly injikovány jen do malé části svalu nemají
pacienti z tohoto pokusu žádný prospěch v podobě nárůstu svalové výkonnosti.
Přesto to považuji za výborný začátek. Studie pokračuje příští rok na více
pacientech, požádali jsme o povolení injikovat větší objem svalu. Šťastné
vanoce!"
30.11.2003
·
Prediction
of Progression of Spinal Deformity in Duchenne Muscular Dystrophy
·
Spinal
fusion and instrumentation for paediatric neuromuscular scoliosis:
retrospective review
·
Postoperative
malnutrition in Duchenne muscular dystrophy
·
Spinal
fusion in patients with Duchenne's muscular dystrophy and a low forced vital
capacity
·
Acute
heart failure during spinal surgery in a boy with Duchenne muscular dystrophy
· Myocardial
cell damage in Duchenne muscular dystrophy
24.11.2003
There's No Muscle in
Some Supplements
Článek pojednává o průzkumu, který provedla společnost ConsumberLab . Týká
potravinových doplňků majících vylepšit svalové schopnosti : kreatin, HMB (hydroxy-methylbutyrate) a
glutamin. Několik úryvků z článku :
·
Ačkoliv se jim říká svaly posilující potravinové doplňky,
chci hned z počátku říct, že nepodporuji užívání těchto doplňků.Ještě
nebylo prokázána bezpečnost jejich použití pro celou populaci a jejich svaly
posilující schopnosti platí jen pro specifické situace. Například u kreatin u
neni dokumentován žádný přínost při čistě aerobních cvičení. Existují menší
studie prokazující jistý užitek, ale to jen ve velmi specifických situací jako
například u pacientů s některými srdečními problémy (congestive heart failure), kde mohou zvyšovat
toleranci k fyzické zátěži a dále u pacientů se svalovými
dystrofiemi, kde mohou zvyšovat svalovou výkonnost. Některé firmy tvrdí,
že tyto látky mohou zvětšovat svaly, předpokládá se ale, že je to způsobeno
zvýšeným zadržováním vody ve svalech, nikoliv zvýšeným množstvím svalstva.
·
Testy ukázaly problémy u většiny kreatinových doplňků
prodávaných ve formě tekutin nebo šumivých tablet, problémy nebyly u kreatinu
ve formě prášku. Jeden nápoj prakticky kreatin neobsahoval a byl kontaminován
látkami vzniklými rozpadem kreatinu, přesto na něm bylo napsáno, že obsahuje
100% stabilního, čistého kreatinu …
·
HMB možná pomáhá
zvětšit svalovou hmotu a zvýšit svalovou sílu při těžkém tréniku, je ale
potřeba udělat víc výzkumů efektivnosti a bezpečnosti než bude možno HMB
doporučit…
·
Všechny glutaminové produkty obsahovaly inzerované
množství glutaminu, ale jeden obsahoval nápisy ve formě porušující FDA (U.S. Food
and Drug Administration) předpisy. Konkrétně uváděl neprokázaná tvrzení, že
snižuje poškození buněk volnými radikály u degenerativních chorob, působí jako
buněčný detoxikant a zvyšuje produkci růstového hormonu. Také neobsahoval
požadované prohlášení, že nebyl odzkoušen FDA a není určen ani k léčbě ani
k prevenci jakékoliv choroby...
20.11.2003:
· A-utrophin up-regulation in mdx skeletal muscle is independent of regeneration
Badatelé z UBC udělali
průlom v léčbě srdce – Kmenové buňky by mohly léčit poškozené srdce u
obětí infarktu
Kmenové
buňky produkované kostní dření, které tělo používá pro vytvoření krvinek, mohou
být využity i pro regeneraci svalů. “Vzhledem k tomu”, říká Dr. Fabio Rossi, člen biomedicinského výzkumného střediska
UBC , “mohou být využity i k umělé regeneraci poškozené svalové tkáně u
pacientů po infarktu, u lidí s cukrovkou nebo svalovou
dystrofií.” Avšak tyto první výsledky
mají ještě hodně daleko k praktickému použití. “I kdybychom měli štěstí a hned
první postup by vedl k úspěšnému použití kmenových buňek, všechny kontroly a
clinické pokusy budou trvat 10 let.”
20.11.2003:
· Stem Cells Can Regenerate Muscle
· Single hematopoietic stem cells generate skeletal muscle through myeloid intermediates
·
Contribution
of hematopoietic stem cells to skeletal muscle
17.11.2003:
Když nervosvalová nemoc ovlivňuje mozek
Margaret
Wahl (Quest)
Některé děti se svalovou dystrofií (MD)
mají kromě fyzických potíží také problémy s poznáváním (poruchy učení) a
emocemi.
Jste-li rodič dítěte s nervosvalovým onemocněním, asi
jste slyšeli něco o mentálním zpoždění, poruchách učení nebo problémech
citových, které doprovázejí svalové
dystrofie a podobné nemoci. Tyto informace byly často prezentovány velmi
neurčitě, takže rodiče, kteří se o tuto problematiku zajímali, nevěděli, zda
psychické problémy dětí jsou důsledky onemocnění nebo ne. Snad nejdůležitější
je, jak těmto dětem pomoci. Některé nervosvalové nemoci mohou souviset s
poznávacími problémy. Nejčastěji se objevují u DMD, BMD a MMD (myotonická
svalová dystrofie). Samozřejmě, že ne každé dítě musí mít poruchy učení, ale
riziko je vyšší než průměr.
DMD – profil poznávání
Řekněme, že u Vašeho 10letého syna s DMD byla
diagnostikována porucha učení, řekněme, že je citově rezervovaný a stále
smutnější ze zhoršujícího se zdravotního stavu. Co můžete dělat?
Většina doktorů Vám řekne, že je těžké nějak
pomoci. Ale existují určité záchytné body. Neuropsycholožka Veronika Hinton z
Columbia University v New Yorku, studuje děti s DMD a BMD. Provádí srovnání
chlapců s DMD a BMD a jejich zdravých sourozenců pomocí několika detailních
testů. Na základě výsledků těchto studií se pokusila sestavit tzv.
"poznávací profily" dětí s DMD.
Děti s DMD byly všeobecně slabé v určitých poznávacích oblastech, které
souvisely se zpracováním nedávné ústní informace. V testech, které se týkaly
opakování číselných posloupností byly mnohem méně úspěšní než jejich
sourozenci. Současní vědci se domnívají, že přibližně 5% chlapců s DMD je mentálně zaostalých a asi třetina má určitý
stupeň duševního poškození nebo poruchy učení. Protože studie byly prováděny v
různých částech USA, podmínky nebyly
srovnatelné a starší literatura dokonce uvádí, že 33% dětí s DMD je duševně
zaostalých. V. Hinton věří, že dokázala identifikovat poznávací problémy - deficit slovní krátkodobé paměti nebo fonologického
zpracování - schopnost zpracovat a odpovědět na právě přijatý podnět .
Tyto problémy jsou zřejmě příčinou poruch učení u všech dětí s DMD a BMD. Ale
na druhou stranu Hinton tvrdí, že mnoho dětí s těmito deficity dokáže díky
vysoké inteligenci tyto poruchy překonat. Ostatní děti s nižším IQ se dostanou
do skupin s poruchami učení ve škole.
Hinton vysvětluje problémy s učením následujícím přirovnáním.
Představte si, že se chcete začít učit nový jazyk. Vstoupíte do místnosti, kde
již všichni tímto jazykem hovoří. Vy sice sem tam zachytíte nějaké slovíčko,
ale nejste schopni zcela porozumět. Snažíte se nějakým způsobem konverzovat -
nedostává se vám některých slov a pokoušíte se vyplnit mezery.
Identifikace problému
Co doporučuje Hinton? Především je třeba provést důkladné
neuropsychologické vyhodnocení poznávacích problémů u Vašeho dítěte pomocí
detailních testů poznávací funkce. Pak
může být vytvořen vzdělávací program pro Vaše dítě. Hinton říká: "
Nejdůležitější věcí, kterou potřebují lidé vědět, o chlapcích s DMD, BMD je, že
většina poznávacích dovedností se
rozvine správně. Každý člověk je v něčem dobrý a něco mu zase dělá
problémy. Ale pokud se díváte na tyto děti jako na skupinu, je zde jedna oblast
(zpracování právě slyšené informace), kde jsou tyto děti více neúspěšné. To
předpokládá existenci nějaké příčiny, která ovlivňuje schopnost učení."
Co je příčinou?
Myslíme si, že to má co dělat s dystrofinem, s proteinem, který chybí ve
svalech chlapců DMD, BMD. Dystrofin je
důležitý ve
svalech, ale nedávné důkazy ukazují i na jeho významné místo v mozku.
Poruchy učení zřejmě souvisí se
svalovou slabostí a je zde jistý důkaz, že souvisí s různými mutacemi v
dystrofinovém genu.
Jaké role hraje dystrofin?
Mark Mehler se zabývá studiem mozku v souvislosti s DMD a BMD. Mehler
tvrdí, že dystrofin se normálně nachází v různých částech mozku - především v
přední části (hippocampus, cerebellum a cerebral cortex). 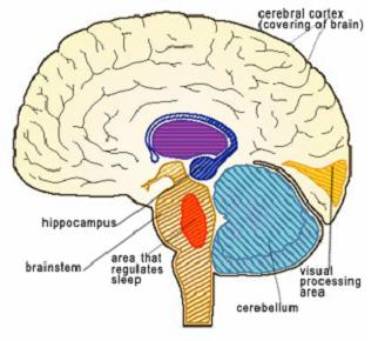
To jsou oblasti, které nejvíce
souvisí s pamětí, pozorností, plánováním pohybu a myšlením. Právě tyto funkce
jsou u chlapců s DMD, BMD nejvíce
zasaženy. Ukazuje se, že v mozku jsou různé formy dystrofinu a způsoby jejich
uspořádání během vývoje jsou tisíckrát komplikovanější než způsob umístění ve
svalu. Jsme na začátku cesty. Mehler si myslí, že emoční projevy jsou důsledkem nedostatku dystrofinu
v mozku. Věc, jako jsou city můžou být úplně mimo pozornost dítěte. Dítě si
může připadat nezapojené nebo postižené - někdy až příliš. Může se někdy
objevit jakési odloučení (izolace) jednotlivce od jeho okolí. Signály v okolí,
které obvykle někoho vyprovokují, že udělá něco rozporuplného, dítě nedokáže
zpracovat, nedokáže Vás pochopit a zapojit se. Naopak dítě nezná hranice, takže
se někdy stane, že dítě s DMD si klidně sedne na klín cizího člověka a nebo si
hraje s jeho tváří. Velká část problémů s poznáváním u DMD,BMD je důsledkem biologie a nesouvisí s vlastním handicapem dítěte. Je
třeba být opatrný na zpětné reakce dítěte a rodiny k nežádoucím efektům DMD a
BMD.
Problémy s udržením pozornosti
Někteří lékaři předepíšou pro
poruchu pozornosti ritalin pro děti s DMD. Veronica Hinton varuje, že diagnóza
deficit pozornosti musí být odlišena od omezené slovní paměti. Jsou to dva
rozdílné problémy. Před tím, než je předepsán ritalin, měla by být vyloučena
varianta, že nejde o poruchu slovotvornou. Pokud je ritalin efektivní, dokáže
zvýšit schopnosti. Mehler doporučuje určit co nejpřesnější diagnózu a
pečlivě monitorovat průběh léčby.
"Jsem člověk, který nevěří na léky v
jakékoliv situaci, ale jsou podmínky, kdy je medikamentózní léčba přínosná.“
Z rodičů se stali experti na vzdělání a obhájci
Tara Wood
Pokud má Vaše dítě poruchy učení i fyzické
postižení způsobené nervosvalovou nemocí, může mu pomoci individuální vzdělávací plán (IEP).
Kromě rehabilitační služby by měl tento plán zahrnovat vzdělávací cíle
přizpůsobené zvláštním schopnostem dítěte. Služby jako fyzioterapie, logopedie , psychologie můžou pomoci dítěti
získat více zkušeností a pomoci při vzdělávání. Pokud jde o postižení fyzické i
poznávací je IEP velmi důležitý. IEP je možné vytvořit průběžně za spolupráce
rodičů, učitelů a lékařů. Plán lze postupně dolaďovat k úplné spokojenosti
rodičů i dětí. (to není případ ČR)
Domácí úkol pro mámu, tátu a učitele
U dětí, které mají omezenou kapacitu paměti, může
pomoci opakování probírané látky v hodině například z magnetofonového záznamu.
Zatímco lékaři a fyzioterapeuti jsou experti na fyzikální nebo poznávací
aspekty dětské nervosvalové nemoci, rodiče mohou být nakonec jediní, kdo zcela
porozumí oběma oblastem. Rodiče by se měli radit jak s neurology, tak i se
speciálními terapeuty a učiteli aby mohli vybudovat mosty mezi nimi. U dětí s
DMD V.Hinton zdůrazňuje přizpůsobení dětského vzdělávacího programu k jeho
silám. V.Hinton např. vypozorovala, že chlapci s DMD jsou celkem dobří v
mechanickém učení ale obtíže jim dělají fonetické přístupy ke čtení obzvláště v
ranných letech.
17.11.2003:
Abstracts from American Heart Association Scientific Sessions 2003, Orlando, 9-12 november 2003
· Impaired Strain Rate Measurements in Patients With Duchenne Muscular Dystrophy
11.11.2003:
09.11.2003:
Blocking
Waste Disposal Restores Dystrophin in Mice
Michael
Lisanti z katedry molekulární farmakologie ( Akademie A.Einsteina New York)
společně s italským výzkumným týmem
nedávno zjistili, že blokování mechanismu likvidace buněčného „odpadu“ může
znamenat cestu k ochraně svalových buněk u DMD.
 V experimentech
s myšima, které produkují pouze fragmenty dystrofinu ( stejně jako řada
lidí s DMD ), Lisanti s kolegy zjistili, že blokování mechanismu likvidace
buněčného odpadu nazývaného proteasomes zřejmě umožní buňkám zachránit a
využít malé fragmenty dystrofinu. Tento svůj objev publikovali v říjnovém
čísle American Journal of Pathology.
V experimentech
s myšima, které produkují pouze fragmenty dystrofinu ( stejně jako řada
lidí s DMD ), Lisanti s kolegy zjistili, že blokování mechanismu likvidace
buněčného odpadu nazývaného proteasomes zřejmě umožní buňkám zachránit a
využít malé fragmenty dystrofinu. Tento svůj objev publikovali v říjnovém
čísle American Journal of Pathology.
Místo likvidace fragmentů dystrifinu ( což je pravděpodobně běžný pochod
v buňkách s DMD defektem ) buňky
léčených myší jej očividně umisťovaly do membrány. A jakmile byly kousky
dystrofinu v buněčné membráně ostatní bílkoviny se také správně připojily a
obnovily pevnost membrány. Autoři studie říkají, že výsledky pokusů představují nový
směr v léčbě DMD.
Použití proteasomových „tlumičů“ by mohlo účinně
blokovat degradaci dystrofinu a tudíž celého dystrofinového komplexu a tak
bychom mohli zlepšit myopatické změny, které jsou normálně pozorovatelné v
kosterním svalstvu myší, které mají poškozený dystrofin.
Použitá látka, která je dostupná jen v laboratorním výzkumu by mohla být
využita i při léčbě rakoviny. Důležité varování je potenciální toxicita
vyřazených buněk.
Normální svalová buňka. Svalová buňka ovlivněná DMD.
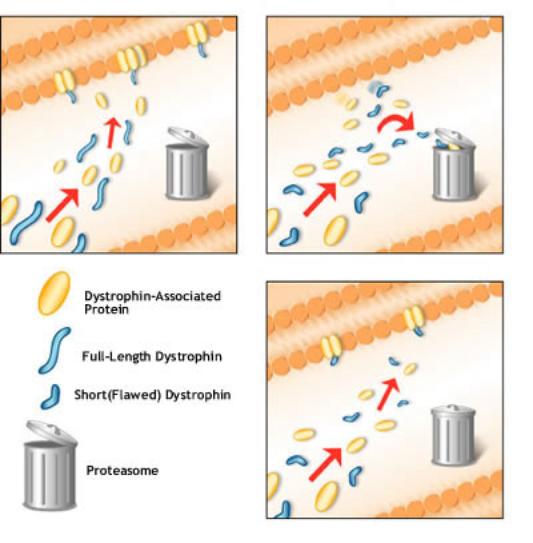
Blokování
odstraňování dystrofinu umožňuje malým fragmentům dystrofinu umístit se na své
místo v blízkosti buněčné membrány.
Dystrophin-Associated
Proteins - komplex bílkovin vázaných na dystrofin
Full-Length
Dystrophin – úplný dystrofin ve správné délce
Short (Flawed) Dystrophin
– zkrácený (vadný) dystrofin
Proteasome –
enzmový komplex, který odbourává mnoho typů bílkovin, řada z nich jsou
regulační bílkoviny, které kontrolují buněčný cyklus
Oxidative Damage Found in Duchenne, Becker MDs, Not in Myotonic Dystrophy
08.11.2003:
Mini-dystrophin
restores l-type calcium currents in skeletal muscle of transgenic mdx mice
Sulfated
polysaccharides of brown seaweed Cystoseira canariensis bind to serum myostatin
protein
Effect
of dietary protein on calpastatin in canine skeletal muscle
06.11.2003:
Correction of the dystrophic phenotype by in vivo targeting of muscle progenitor cells
Long-term noninvasive ventilation in children and adolescents with neuromuscular disorders
4.11.2003
Zpráva z konference MDA
: Kardiomyopatie u svalové dystrofie
Následující
text je shrnutím z několika zpráv přednesených na konferenci, jde o doporučení
jak péčovat o pacienty.
Duchenne
MD
- echokardiogram
a elektrokardiogram v okamžiku diagnostikování
- kardiologické
vyšetření před každým chirurgickým zákrokem a každé 2 roky do 10 let,
každoročně po desátém roce
- při léčbě
respiračních dysfunkcí současně kontrolovat srdce
- léčba
angiotensin-converting enzyme (ACE) inhibitory, přidat beta blokery když
abnormality začnou růst
Becker MD
- echokardiogram
a elektrokardiogram v okamžiku diagnostikování
- kontrola
kardiomyopatie nejméně každých pět let
- léčba ACE
inhibitory a případně beta blokery v případě nalezení abnormalit
- zvážení
srdeční transplantace
Ženy
přenašečky DMD/BMD
- echokardiogram
a elektrokardiogram v okamžiku diagnostikování nebo po dosažení věku 16 let a pak nejméně každých 5 let,
abnormality vyhodnocovat častěji v případě symptomů na kosterním
svalstvu či srdečních symptomů
- léčba ACE
inhibitory a případně beta blokery v případě nalezení abnormalit
- zvážení
srdeční transplantace
29.10.2003 :
Creatine Supplements May Improve Muscle Strength in Young Children With DMD
Martha Kerr, Medscape Medical News
Kreatin může
zlepšit svalovou výkonnost u malých dětí s DMD
Malé děti s DMD vykazují větší
svalovou sílu, funkčnost a pomalejší postup nemoci pokud berou kreatin oznámili
badatelé na 128 výročním setkání Americké neurologické asociace.
Na základě výsledků studií na
zvířatech s DMD, které ukázaly, že glutamin a kreatin chrání před ztrátou
svalové výkonosti, byla provedena studie na 60 dětech s DMD ve věku od pěti do
devíti let.
Vedoucí výzkumu Diana M. Escolar
z Children's National Medical Center at George
Washington University in Washington, D.C. náhodně rozdělila děti do 3 skupin.
První skupina dostávala 5g kreatinu a placebo dvakrát denně, druhá skupina
glutamin 0,3mg/kg a placebo dvakrát denně, třetí jen placebo dvakrát denně. Dr.
Escolar k tomu dodavá, že byly porovnávány kreatin versus placebo a glutamin
versus placebo ale ne kreatin versus glutamin. Hlavní závěr byl učiněn na
základě měření svalové výkonnosti ( MMT, 34 svalových skupin ), dále byla
vyhodnocována funkčnost na základě různých fyzických aktivit ( QMT, 7 svalových
skupin ). Byl zjištěn velmi
odlišný výsledek u 30 dětí v „mladší“ skupině ( mezi 5 a 7 roky )
a 30 dětmi ve “starší” skupině ( 7 až 9 let ).
V této šestiměsíční
studii se u všech tří studovaných skupin skóre MMT příliš nelišilo. Ale v QMT
skóre děti ze skupiny, která brala jen placebo, vykazovaly větší zhoršení v
porovnání s dětmi z obou léčených skupin. Děti užívající kreatin vykazovaly
menší zhoršení než děti užívající glutamin. Děti z mladší skupiny měly vyšší
skóre ve funkčních testech jako bylo stání, vztávání a běh než starší děti
užívající kreatin.
Mám teorii, která to
vysvětluje, říká Dr. Escolar. Tyto látky zvyšují svalovou energii. Mladší děti
mají svaly, které reagují více na zvýšené množství energie než starší děti.
Nepotřebují totiž více síly ale energie. Pro starší děti se zvýšení síly
transformuje do zvýšení funkčnosti. Je tedy možné, že energetické potravinové
doplňky dokonce mohou zpomalit postup DMD.
Upozornila také na to,
že kreatin a glutamin mají velmi malé nepříznivé účinky. “Jestliže rodiče
chtějí jít a koupit tyto potravinové doplňky nebudu se toho obávat.”
Plasmid-Based Gene Therapy for Muscular Dystrophy Succeeds in Preclinical Study
Reuters Health Information
27.10.2003 :
Proteasome
inhibitor, Sharon Hesterlee, Ph.D.
Hi all,
We have
been working with a U.S. investigator on proteasome inhibitors and DMD--I
agree that the approach is very interesting and it is particularly important
that there is already a proteasome inhibitor in development in the U.S. We are
in the process of picking a lead candidate for our new Bench-to-Bedside
initiative (designed to get drugs out of the laboratory and into clinical
testing more quickly), and proteasome inhibitors are on the short list.
The
good news is that we are having trouble narrowing the field for a lead
therapy because there are so many promising approaches coming out of
laboratories now. We just want to make sure that we are prepared to
suceed, i.e., that we have all the pieces in place to move new drugs through
the clinical testing process as efficiently as possible.
Best
Wishes,
Sharon
Sharon
Hesterlee, Ph.D.
Director
of Research Development
Muscular
Dystrophy Association
(520)
529-5433
Zdravím všechny,
Pracujeme na tlumičích
proteasome ( proteasome inhibitors ) a DMD.
Nyní jsme ve stadiu shromažďování a hledání kandidáta pro naše nové úvodní zkušební testy (dostat rychle léky z
laboratoře do klinického testování ) a proteasome inhibitory jsou na užším
seznamu těchto látek.
Dobré zprávy jsou, že máme
na seznamu tolik vhodných a slibných látek, že je těžká volba výběru. Chceme se
jen ujistit, že jsme dobře připraveni na efektivní klinické testy nových léků.
Sharon Hesterlee, Ph.D.
Ředitelka výzkumu MDA
Asociace svalových dystrofií
20.10.2003
:
HealthDayNews
Vědci jsou zase o krok blíž
k efektivní genové terapii pro MD. Výzkumníci z lékařské fakulty ve Standfordu
zkouší použití genetického materiálu tzv. "plazmidů" a bílkoviny zvané "integrase" k
doručení nového genu do svalových buněk. Jde o nevirový přenos genetického
materiálu.
Jejich technika se zdá být
bezpečná, ale musí být obezřetní, protože jejich experimenty na laboratorních myších jsou ještě v počátečním
stadiu a použití na lidech bude
uváženo. Výsledky pokusů budou zveřejněny 21.10.2003 na setkání Neurologické
asociace v San Francisco.
"Objevily se
schůdné přístupy pro nevirový přenos u genové terapie" řekl DR. Thomas
Rando, profesor neurologie na Standford
Univerzitě a člen Lékařského centra
Palo Alto. " Jednoduchou
plazmickou DNA je snadné a levné
připravit."
MD je dědičná choroba
způsobená mutací genu. Existuje mnoho typů MD, např. Duchenne nebo Becker, pro
oba typy je charakteristické ochabování svalstva. Některé formy MD jsou
smrtelné.
Chybějící nebo zmutovaná
část genu v MD ovlivňuje produkci bílkoviny zvané dystrofin. Jakákoliv genová
terapie by musela být schopná doručit dystrofinový gen do všech svalových
buněk, které jsou postiženy.
Vědci se rozhodli
nejprve vyzkoušet gen zvaný luciferase.
Výhodou tohoto genu je, že vysílá světlo,
které lze zachytit pomocí speciální kamery. Tento způsob vědcům umožňuje
vidět, jestli se gen dostane do buňky.
Vědci vpíchli plasmidy
obsahující luciferasi do jedné nohy laboratorní myši a integrasi plus plasmidy
s luciferásí do druhé. Brzy po vstřiku obě nohy vykazovaly znaky přítomnosti
genu s luciferasí. Pozděj ale noha bez integrase již neměla příznaky luciferase
genu. Noha s integrasí dále jevila znaky luciferase genu, ukázalo se, že gen se
dostal do buněčné DNA.
Dr. Rando řekl, že další
krok bude představovat zkouška, zda tato technika bude účinná i v dystrofinovém
genu.
Nejvýznamnější výzvou je
pro vědce možnost doručit geny ke všem svalových buňkám. V současnosti to lze
jen místně pomocí vstřiku přímo do svalu.
Další obavy jsou z
nežádoucích vedlejších účinků, i když ještě žádné neobjevili. To jsou především
problémy genových terapií, které používají k přenosu genetického materiálu
viry. Zatímco viry jsou celkem efektivní při přenosu do buněk, tělo je vybaveno
schopností vytvářet imunitní odpověď organismu proti virům. Viry jsou také malé
a často nemouhou přenést větší léčebné geny.
Sharon Hesterlee, ředitelka
výzkumu MDA řekla: "Tato studie
je přínosná právě díky nevirovému přenosu genu. Je to velice zajímavá studie a
pokrok v používání plazmické techniky , která je velice mladá."
Říjen 2003
:
Utrophin
Utrophin
je protein, který se velice podobá dystrofinu. Jeho gen je umístěn na chromozómu 6 a má 75 exonů.
Utropin je o 7 % kratší než dystrofin. Chlapci s DMD nemají žádný dystrofin ale
v malém množství mají utrophin na svých
nervosvalových spojeních, kde dochází k nervovému přenosu do svalů. Kdyby v
těle chyběl i utrophin, průběh nemoci by byl mnohem horší.
Pomocí genetické manipulace
u myší s MD bylo vytvořeno větší
množství utrophinu ve svalech. To zabraňovalo vzniku dystrofických symptomů.
Takže, utrophin je schopen zastoupit dystrofin, pokud je přítomen ve větším
množství. Použité myši byly geneticky upravené, to nelze použít u lidí.
Nicméně následuje další strategie, jak zvýšit
obyčejně nízký obsah utrophinu pomocí "posílení" aktivity tohoto
genu. K tomu je třeba nějaká aktivující substance , lék nebo jiná syntetická či
přírodní látka.
Během loňského roku se
objevily tisíce nových substancí. Mnoho z nich je testováno na kultivaci
svalových buněk u mdx myší, zda můžou aktivovat gen pro luciferase. Luciferase
produkuje slabé světlo a je vhodnější k testování než utrophin.
Kay Davies a její
spolupracovníci našli okolo 100
sloučenin, které zvyšují produkci luciferase. Vědci nyní vědí, že jejich
systém funguje.
Tyto účinné substance jsou
dále chemicky upraveny a všechny se
testují ve svalových buněčných
kulturách, ty nejúčinnější na živých myších.
Výhody zvýšení produkce
utrophinu jsou:
Látka, která aktivuje
zvýšení by mohla být aplikována nitrožilně do krevního oběhu, takže by se
dostala do všech svalů v těle.
Imunitní systém by
rozpoznal utrophin jako známou látku (u dětí s DMD v malých množstvích), proto
se neočekává žádná nežádoucí odezva imunitního systému.
Pokud se najde látka, která
dokáže zvýšit produkci bílkoviny, pak by měla fungovat i v ostatních genech.
Než dojde k testům na chlapcích, musíme si být jisti, že žádné nežádoucí účinky
látka nevyvolává.
Další pokusy :
-
Množství utrophinu se zvětšilo po použití steroidního hormonu, výtažkem
z rostliny tradiční čínské medicíny, při chronickém zánětu ve svalech,vyvolaným
proteinem heregulin, aminoacidem.
-
L-arginine a transferem utrophinového genu do psa s DM.
-
Další forma utrophinu, velice podobný B-utrophin byl identifikován
nedávno v krevním řečišti. Ale pouze normální A-utrophin je přítomen ve svalech
a může částečně nahradit dystrofin zvýšenou produkcí.
Závěry práce profesora Alfreda Strachera z Univerzity v New
York o leupeptinu
Leupeptin je tripeptid,
který se skládá ze tří amino-kyselin. Blokuje aktivitu enzymu calpain. U DMD
calpain ničí bílkoviny ve svalových buňkách, jestliže je přítomen vápník. V pokusech na myších a opicích došlo k
potlačení svalové degenerace. Ve spojení leupeptinu s karnitinem se účinky
dokonce zvýšily. Tato studie na myších právě začala a bude dokončena za půl
roku. Šestiměsíční pokus s leupeptinem na psech s DM je dokončen a během
několika týdnů budou k dispozici výsledky.
Jestliže pokusy na psech
dopadnou dobře, můžeme očekávat klinické studie na pacientech v příštím roce.
Na závěr ještě uvádím, že
leupeptin nemusí být vstřikován ale může se polykat jako lék.
Gentamicin
- ovlivnění pacientů s předčasným ukončením čtení genetického kódu.Předběžné
výsledky
Politano L, Nigro G, Nigro
V, Piluso G, Papparella S, Paciello O, Comi LI. (Department of Clinical and
Experimental Medicine and Surgery, Section of Cardiomyology and Medical Genetics,
2nd University of Naples, Italy. luisa.politano@unina2.it )
Cílem studie bylo zkoumat,
zda gentamicin je schopen obnovit
funkci v příčně pruhovaném svalstvu u
pacientů s DMD s předčasným ukončením
čtení kódu (PSC).
Byli vybráni 4 pacienti s DMD
(chodící nebo na vozíčku ne déle než 4 měsíce), kteří měli mutaci
dystrofinového genu označovanou jako předčasné ukončení čtení kódu pro tvorbu
bílkoviny dystrofin.
Pacienti dostávali během
dvou šesti denních cyklů gentamicin sulfát v intervalu 7 týdnů (podle
odsouhlaseného protokolu schváleného etickým výborem z Univerzity v Neapolu) .
Svalová biopsie byla
provedena po druhém cyklu pokusu,
vzorky byly analyzovány immuno - histochemicky a western blot testem.
Změny v kosterním svalstvu byly monitorovány pomocí dynamických testů hodnoty Creatin Kinase na začátku a na konci
léčby, srdeční sval a dýchací funkce byly sledovány pomocí elektrokardiografie
a echokardiografie, akustickým denzitometrem a
spirometrem.
U tří pacientů došlo k pozitivním efektům. Výsledky pokusů
ukázaly, že gentamicin může obnovit
dystrofin u pacientů s "nonsense" mutací (PSC). Zvyšuje
se možnost, že gentamicin se stane prvním lékem na DM u pacientů s PSC
(premature stop codon).
Evropská
studie zjistila prospěšnost kreatinu u Duchennenovy a Beckerovy svalové
dystrofie
QUEST Volume 10, Number 4, JULY/AUGUST 2003
http://www.mdausa.org/publications/Quest/q104resup.cfm#europecreatine
Badatelé v Belgii a Francii právě dokončili studii 15
chlapců s Duchennenovou a Beckerovou svalovou dystrofii a zjistili, že tento
potravinový doplněk zpomaluje tuhnutí kloubů, zvyšuje sílu a odolnost proti
únavě.
Dále se zjistilo, že kreatin zvýšil hustotu kostí o
3% u těch pacientů, kteří nepoužívaji invalidní vozík Žádné nepříznivé účinky
kreatinu nebyly pozorovány.
Magali Louis a kolegové publikovali tyto výsledky v
květnovém vydání Muscle & Nerve. Tři měsíce podávali denně osmi chlapcům
orálně kreatin a dalším sedmi placebo. Po dvou měsících, během nichž
nedostávali jiné léky, první skupina dostala placebo a druhá kreatin takže
každý dostával kreatin po dobu tří měsíců.
Ačkoliv schopnost kreatinu zvýšit svalovou výkonnost
je zřejmě hlavním důvodem, badatelé se domnívají, že může mít i jiný svaly
podporující účinek.
Autoři této studie říkají, že kreatin se mohl
uplatnit prostřednictvím signálových cest (signaling pathway ) v buňkách, které
ovlivňují jak svaly tak kosti. Dále dodávají, že účastníci, kteří brali kreatin
možná byli aktivnější což je prospěšné pro hustotu kostí.
Poslední studie kreatinu u myotonické svalové
dystrofie typu 2 (type 2 myotonic muscular dystrophy ) naznačuje, že by mohl
pomoci i snížit bolesti u této choroby.
MDA podporované studie kreatinu jsou prováděny i ve
Spojených státech, Kanadě a jinde. Tyto pokusy jsou již hotovy a data jsou
analyzována.
Krevní test pro určení DMD -duben 2003 (Flanigan KM)
Vědci vyvinuli jednoduchý krevní test, který je schopen odhalit svalovou
dystrofii v 95% případů. Dosud zůstávaly u 35% pacientů neodhaleny mutace
způsobující DMD. Pacienti proto museli podstupovat nepříjemné testy (svalová
biopsie), které s sebou přináší jistá rizika a zatížení. Nyní je možné při
použití nové metody (SCAIP Single Condition Amplification/Internal Primer
Sequencing) odhalit všechny případy DMD.
Dystrofinový gen (DG) je nejdelší známý lidský gen. Známe několik různých typů
mutací spojených s DMD. Nový krevní test (SCAIP) umožňuje genetikům seřadit
celý DG, najít mutace a potvrdit DMD. S aktuálně dosptupnými genetickými testy
nyní můžeme hledat i jiné typy mutací. Je velká naděje, že tento test bude
široce dostupný na klinikách (zatím Univerzita Utah, USA).
Dosud užívaný krevní test hledal chybějící části DG – tzv exony . Exon je
oblast uvnitř genu, která obsahuje důležité části genetického kódu. 60% případů
DMD je způsobeno vymazáním (delecí) jednoho nebo více exonů uvnitř DG. Dosud
byla překážkou enormní délka DG pro otestování všech mutací. Před vývojem SCAIP
nemohl genetik objevit 35% mutací a musela být provedena svalová biopsie nebo
další testy.
Vývoj nového testu je důležitý nejen pro diagnostiku pacientů, ale i pro
zachycení přenosu z matky na dítě.
„Pokud chceme s touto nemocí úspěšně bojovat, potřebujeme být schopni rozpoznat
specifické mutace „Potřebujeme umět identifikovat specifické mutace, abychom
byli schopni pomocí příslušné terapie opravit tyto defekty. Tento test je
prvním důležitým krokem, ale většina práce je před námi.“ (Dr. Flanigan)
Dr. Flanigan a jeho kolegové ze tří výzkumných center vytváří rozsáhlou
databázi pacientů,obsahující klinické a genetické informace velkých skupin
pacientů s DMD. Vědci doufají,že podrobná genetická informace o těchto
pacientech pomůže výzkumníkům generovat nové hypotézy a eventuálně nové způsoby
léčby.
„Jako vědec jsem velmi vzrušený a šťastný, že můžu ukázat novou cestu k
rychlému určení diagnózy a odstranit tak nejistotu rodičů, kteří dosud nemají
správnou odpověď.“ (odkaz: „Rychlá přímá sekvenční analýza DG“ American Journal
of Human Genetics)
Francouzská studie přenosu genu u DMD nebo BMD vypadá bezpečně a
slibně !
Výzkum – léčba >> Francouzská studie přenosu genu
AFM (Asociace Myotoniků Francie) ve spolupráci s Transgene ( Biotechnologická
společnost Strasbourgh) oznámili, že nevirový přenos v genové terapii DMd a BMD
se jeví bezpečně a je příslibem pro budoucí možnou léčbu Duchenn/Becker svalové
dystrofie. Oznámení bylo učiněno na setkání Americké společnosti genové terapie
ve Washingtonu. Projektu se účastnil spolupracvník MDA Jon Wolff (Univerzita
Wisconsin v Madison). Wolff rozvinul velkou část strategie používané pro
doručení „léčebného genu“, který nese instrukce pro důležitý svalový protein
dystrofin. Právě dystrofin chybí ve svalech pacientů s DMD nebo BMD.
Dystrofinový gen byl poprvé identifikován v roce 1986. V pokusech, jejichž
výsledky byly nyní oznámeny, vědci použili strategii přenosu holé DNA, která
spojí požadovaný gen do kusu genetického materiálu zvaného plazmický.
Výzkumníci vstříkli kombinaci plazmid dystrofinové konstrukce (PDK) přímo do
svalu u 15 chlapců s DMD nebo BMD. Účastníci pokusu byli rozděleni do tří
skupin. První dvě po šesti a třetí skupina po třech. Chlapci v prvních dvou
skupinách dostali jednu injekci s 200 mikrogramy nebo 600 mikrogramy PDK,
zatímco chlapci ze třetí skupiny dostali dvě injekce 600 mikrogramů během 2
týdnů. Po 21 dnech od vstříknutí vědci zkoumali vzorky. Malé množství
dystrofinu patrně vyrobeného v důsledku aplikování PDK se objevilo mezi 1 až 10
% svalového vlákna u poloviny chlapců v prvních skupinách a u všech ze třetí
skupiny. Dystrofin byl přítomen jen v malé oblasti kolem vpichu. Vědci věří, že
výroba dystrofinu asi v 20% svalové membrány může způsobit významné rozdíly ve
funkci svalu. Neobjevily se žádné známky reakce imunitního systému – což je
znamenitý výsledek.
AFM a Transgene nepřestává zdokonalovat systém ne-virového transferu DNA.
Dřívější genová terapie se snažila doručit opravený gen prostřednictvím viru,
což mělo za následek nepříznivou odezvu imunitního systému.
„Tyto výsledky poprvé demonstrují, že je možné lokálně vytvořit dystrofin u
pacientů s DMD nebo BMD pomocí plazmidů obsahujících lidský dystrofinový gen.“
* výrazy vytištěné kurzívou
nepřekládáme z důvodu nedostatečné znalosti odborné terminologie
Tyto stránky jsou určeny nejen rodičům ale i lékařům. Vše co
považujeme za důležité pro rodiče se budeme snažit přeložit do češtiny.
Omlouváme se za případné nepřesnosti při překladu a děkujeme za pochopení.